2023-01-06 10:57:23 č«Ő(wšŽ)TżŒÔŸW(wšŁng) 
 ÎÄŐÂíÔŽŁșÎŽÖȘ
ÎÄŐÂíÔŽŁșÎŽÖȘ
(Îßxî})ÎïÙ|(zhšŹ)”ÄœY(jišŠ)(gš°u)Q¶šĐÔÙ|(zhšŹ),ŁŹÎąÁŁég”ÄÏໄŚśÓĂÁŠÔœ(qišąng)ŁŹÈÛüc(dišŁn)Ôœžß,ĄŁÒ»Đ©Ńő»ŻÎï”ÄÈÛüc(dišŁn)ÈçϱíŁș
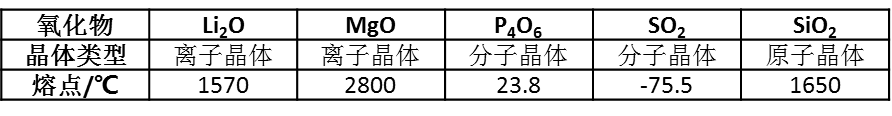
ÏÂÁĐßxí(xiš€ng)ÖĐ,ŁŹČ»ÄÜœâáŃő»ŻÎïÈÛüc(dišŁn)ŽæÔÚČîź”ÄÊÇŁș
A.·ÖŚÓŸ§ówÖДČśÓĂÁŠÊÇÏàŠ(dušŹ)Ę^Èő”Ä·ÖŚÓégŚśÓĂÁŠ
B.ëxŚÓŸ§ówÖДČśÓĂÁŠÊÇÏàŠ(dušŹ)Ę^(qišąng)”ÄëxŚÓæI
C.ÔŚÓŸ§ówÖДČśÓĂÁŠÊÇÏàŠ(dušŹ)Ę^Èő”ÄčČr(jiš€)æI
D.Li2OÖĐ”ÄëxŚÓæIÈőÓÚMgO”Ä
œâÎö
”ÚÒ»ČœŁŹŽ_¶šî}ĐÍ,ĄŁ
±Ÿî}żŒČ黯W(xušŠ)ÖĐ”ÄÈÛüc(dišŁn),ĄŁ
”Ú¶țČœŁŹ·ÖÎöÔÀí,ĄŁ
![]()
Aí(xiš€ng)Łș·ÖŚÓŸ§ówÊÇ·ÖŚÓégÍšß^·ÖŚÓégŚśÓĂÁŠ(·ÖŚÓégŚśÓĂÁŠÓÖĂû·¶”ÂÈAÁŠ,ŁŹ¶űäæIČ»ÊÇ»ŻW(xušŠ)æIŁŹÊÇÒ»·NÌŰÊâ”Ä·ÖŚÓégŚśÓĂÁŠ,ŁŹÙÓÚ·ÖŚÓégŚśÓĂÁŠ)(gš°u)łÉ”ÄŸ§ów,ŁŹÈç±íÖĐ”ÄșÍŁŹŚśÓĂÁŠĘ^Èő,ŁŹÈÛ·Đüc(dišŁn)Ę^”Í,ŁŹÒòŽËżÉÒÔœâáŃő»ŻÎï”ÄÈÛüc(dišŁn)Čîź;
![]()
Bí(xiš€ng)ŁșëxŚÓŸ§ówÊÇŐꥹŰ(fšŽ)ëxŚÓÍšß^ëxŚÓæIœY(jišŠ)șÏĐÎłÉ”ÄŸ§ów,ŁŹÈç±íÖĐ”ÄșÍMgO,ŁŹŚśÓĂÁŠĘ^(qišąng)ŁŹÈÛ·Đüc(dišŁn)Ę^žß,ŁŹÒòŽËżÉÒÔœâáŃő»ŻÎï”ÄÈÛüc(dišŁn)Čîź;
![]()
Cí(xiš€ng)ŁșÔŚÓŸ§ówÊÇÏààÔŚÓÖźégֻ͚ß^čČr(jiš€)æIœY(jišŠ)ș϶űłÉ”ÄŸ§ów,ŁŹÈç±íÖДģŹŚśÓĂÁŠĘ^(qišąng),ŁŹÈÛ·Đüc(dišŁn)Ę^žß,ŁŹCí(xiš€ng)±íÊöće(cuš°)Ő`ŁŹČ»ÄÜœâáŃő»ŻÎï”ÄÈÛüc(dišŁn)Čîź;
![]()
Dí(xiš€ng)ŁșșÍMgOŸùéëxŚÓŸ§ów,ŁŹëxŚÓégÏໄŚśÓĂÁŠŸùéëxŚÓæI,ŁŹMgO”ÄÈÛüc(dišŁn)Ę^žßŁŹžùț(jšŽ)“ÎąÁŁég”ÄÏໄŚśÓĂÁŠÔœ(qišąng),ŁŹÈÛüc(dišŁn)Ôœžß”,ŁŹÆäëxŚÓæIĘ^(qišąng),ŁŹÒòŽËżÉÒÔœâáŃő»ŻÎï”ÄÈÛüc(dišŁn)ČŁ
ÒòŽË,ŁŹßxńCßxí(xiš€ng),ĄŁ

ÏàêP(gušĄn)È(nšši)ÈĘÍÆË]Łș
ÉÏÒ»ÆȘŁșĂżÈŐÒ»î}ÖźĆĐàŁš2023Äê1ÔÂ3ÈŐŁ©
ÏÂÒ»ÆȘŁșĂżÈŐÒ»î}ÖźĆĐàŁš2023Äê1ÔÂ5ÈŐŁ©

ó(bš€o)ĂûlŒț?
λßxń?
čPÔżÆÄż?
ĂæÔ·œÊœ?
......

 ÔÚŸżÍ·țĄÁ
ÔÚŸżÍ·țĄÁ

üc(dišŁn)ôËùĐèÙYÁÏ,ŁŹßŽaîI(lš«ng)ÈĄ








ŐĐżŒč«žæżŒÔŽóŸVÂλ±íó(bš€o)ĂûÈëżÚÊ(zhšłn)żŒŚCŽòÓĄżŒÔr(shšȘ)égłÉż(jš©)ČéÔĂæÔĂûÎäÓĂč«ÊŸżŒÔżìÓ
ó(bš€o)żŒÁśłÌó(bš€o)żŒŽđó(bš€o)żŒlŒțÂÄÜœéœBŐțČß·šÒ(guš©)ó(bš€o)żŒ”(shšŽ)ț(jšŽ)·ÖÎövÄêżŒÇé